Cómo luchar contra el auge de las superbacterias
En 2050, las superbacterias matarán a 10 millones de personas en el mundo. ¿Qué podemos hacer para evitarlo?
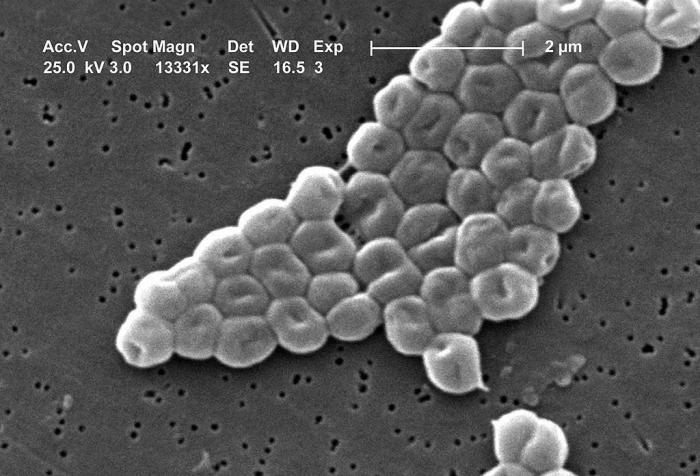
Como en uno de esos carteles de comisaría que muestran los rostros de los delincuentes más buscados, aparecen desde esta semana un grupo de doce bacterias multirresistentes que son, para la Organización Mundial de la Salud, el enemigo público número 1. La publicación de las identidades de esta banda de microorganismos, en la que están Acinetobacter baumannii, Pseudomonas aeruginosa, Enterobacteriaceae o Enterococcus faecium, es un paso más en la alerta mundial de la OMS sobre patógenos resistentes al arsenal de antibióticos con el que cuenta la medicina.
Cada una de las bacterias que aparece en la orden de "busca y captura" de la institución sanitaria, en la que también están Staphylococcus aureus, Helicobacter pylorio Campylobacter, causa ya miles de muertos al año en el mundo. Es por eso que las previsiones de la OMS sobre la mortalidad relacionada con estas superbacterias parecen cada vez menos exageradas: en 2050, estos microorganismos y sus enfermedades asociadas matarán a 10 millones de personas al año en el mundo. O lo que es lo mismo, matarán a más gente que el cáncer y la diabetes juntas.
"El CDC (Center for Diseases Control, algo así como el Instituto de Salud Carlos III norteamericano), declaró en 2013 que habíamos entrado en la "era post-antibiótica"", señala el doctor Víctor Jiménez Cid, experto de la Sociedad Española de Microbiología y profesor de la Universidad Complutense de Madrid (UCM). No todos los investigadores están de acuerdo con una afirmación tan catastrofista, pero sí concuerdan en que nos encaminamos a un escenario complicado: "Sería como volver a los tiempos previos a la Primera Guerra Mundial, en la que habría un enorme aumento de la mortandad por infecciones y un aumento considerable de las muertes neonatales", apunta el doctor Bruno González Zorn, especialista en Microbiología y Biología Molecular de la UCM y experto en la resistencia antibiótica.
Perderíamos, por ejemplo, buena parte del terreno ganado durante las últimas décadas en cuanto a esperanza de vida. La resistencia antimicrobiana, pues, es una amenaza real para la salud global y la alerta lanzada por la OMS "no está injustificada". Pedro García, investigador del Centro de Investigaciones Biológicas del CSIC, alerta de que "cada vez son más los clones multirresistentes [los genes bacterianos que soportan los antibióticos] y cada vez leeremos más noticias sobre muertes por esta causa".
El doctor García ha apuntado a una de las circunstancias que ha contribuido a situarnos en este escenario y, al mismo tiempo, la que hará que sea difícil salir de él en el corto plazo: la capacidad evolutiva de las bacterias. En eso inciden también los doctores Jiménez Cid y González Zorn. La bacterias, explica el primero, "son capaces tanto de mutar sus genes como de transferir entre distintas especies genes o grupos de genes donde se codifica la base molecular de la resistencia". O lo que es lo mismo, como resume el segundo: "Las bacterias son la forma de vida más exitosa de la Tierra. Se reproducen muy rápido, mutan muy rápido y se intercambian ADN de unas a otras".
Así es cómo han ido desarrollando su resistencia a los antibióticos, aunque no sólo las leyes evolutivas de Darwin han contribuido a la velocidad del proceso. El abuso de los antibióticos y el mal uso de los mismos también ha puesto su granito de arena en el surgimiento de estas superbacterias. El mecanismo no es difícil de entender: "La sobremedicación, el mal uso clínico y el abuso de antibióticos en la producción animal han expuesto a nuestras poblaciones microbianas a los antibióticos seleccionando clones resistentes en nuestro organismo y en el medio ambiente", diagnostica el doctor Jiménez Cid.
El doctor García, en esa línea, apunta a una circunstancia que puede resultar familiar a todos: "Cada antibiótico tiene unos ciclos y una posología que no son caprichosos. Es importante cumplirlos y no hacer lo que solemos hacer, que es dejar los tratamientos a la mitad cuando empezamos a encontrarnos mejor. Esa posología está pensada para acabar con el 99,9% de las bacterias, pero si detenemos el tratamiento indebidamente, sólo destruiremos el 99%. El 1% restante no sólo sobrevive, sino que evoluciona como resistente y además prolifera". Es a través de esos clones resistentes como las bacterias han desarrollado mecanismos para sobrevivir a los cañonazos antibióticos.
Tal y como señaló unas líneas más arriba el doctor Jiménez Cid, uno de los cuarteles generales de la resistencia antimicrobiana son las granjas animales. Pero el otro son los hospitales, más en concreto, las Unidades de Cuidados Intensivos. Es en ellas donde el núcleo duro de la lista de la OMS, llamado grupo ESKAPE (Enterococcus faecium,Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumanii, Pseudomonas aeruginosa y Enterobacter spp) se ha hecho cada vez más intratable. "En el ámbito hospitalario, los pacientes están especialmente expuestos por su estado de base (tratamientos inmunosupresores, postoperatorios, quemados...). La debacle sería que estas bacterias escaparan de los hospitales y se propagaran libremente por las poblaciones".
No parece que vaya a ocurrir, puesto que estas bacterias "oportunistas" no suelen atacar a individuos sanos. Pero la dificultad para controlarlas en el ámbito hospitalario y la falta de medios para luchar contra otras bacterias que están en la calle y que son multirresistentes, como la tuberculosis, tienen el mismo talón de Aquiles, otra de las razones que explican la alarma: la falta de investigación. "Todas las familias de medicamentos que actualmente utilizamos contra las bacterias", explica el doctor González Zorn, "se descubrieron en un período aproximado de tres decenios, hasta los sesenta/setenta del siglo XX. Desde entonces, la intensidad de la investigación ha disminuido".
Víctor Jiménez Cid incide en ese aspecto: "Quienes tienen el potencial de descubrir nuevos antibióticos (las grandes farmacéuticas, esencialmente) no encuentran atractiva la inversión millonaria en I+D en este campo, puesto que son veinte veces más rentables en el mercado los medicamentos que tratan trastornos neuromusculares crónicos, por ejemplo". Y concluye: "Quince de las 18 compañías farmacéuticas más grandes han abandonado la I+D en antibióticos, mientras que los grupos académicos que dependen de dinero público han sufrido los efectos de la crisis".
El doctor García cree que "será muy difícil que haya una reversión total de la situación, pero quizás con buenas prácticas consigamos bajar las tasas de multirresistencia de bacterias". Jiménez Cid comparte su optimismo: "En los últimos años hemos mejorado sensiblemente en la percepción social del problema, al menos en los países desarrollados. Se han desplegado campañas más o menos efectivas sobre el uso racional de antibióticos, para limitar su prescripción a cuando son realmente necesarios. Hoy en la Unión Europea no deberíamos tener acceso a estos fármacos sin receta médica, su uso en producción agropecuaria es ilegal, etc. Por tanto, hemos ganado terreno en educación de la población, aunque es notorio que son comunes las infracciones en este campo".
Pero la batalla más importante contra las superbacterias es la que deben dar los medicamentos, y a pesar de la falta de inversión y los recortes, existen diferentes estrategias para aplastar la resistencia antimicrobiana. Cada uno de los tres especialistas consultados, de hecho, dedica sus esfuerzos a una línea diferente de investigación para hallar la manera de reducir a las superbacterias.
Víctor Jiménez Cid es uno de los responsables en España de Small World Initiative (SMI). Gestado en la Universidad de Yale, el proyecto "sigue una estrategia de crowdsourcing" que involucra a jóvenes entre 15 y 18 años: "Eligen un suelo de un hábitat concreto, exploran su diversidad microbiana y seleccionan aquellos microorganismos que muestran actividad inhibitoria sobre bacterias similares biológicamente a las ESKAPE. Ellos mismos hacen todo esto en el laboratorio de su instituto con el apoyo de profesores e investigadores de la Universidad". De esa manera, ahorran trabajo de campo a los grupos que trabajan en el desarrollo de nuevas moléculas y, al mismo tiempo, se ven atraídos por la investigación en ese campo. Durante el primer curso de SMI en España, han participado en él más de 100 estudiantes universitarios y al menos 500 estudiantes de la ESO o bachillerato.
El día de mañana, es posible que algunos de esos estudiantes forme parte o incluso dirija proyectos de investigación como los que lleva a cabo Bruno González Zorn. El doctor ha dedicado buena parte de su investigación a encontrar la manera de impedir la evolución darwiniana de las bacterias y, de ese modo, frentar la multirresistencia: "Son estrategias novedosas, que persiguen el desarrollo de moléculas que interfieren en la transferencia de ADN de una bacteria a otra, o que impidan la captación de genes de resistencia o incluso que ralenticen la capacidad mutacional de los microorganismos".
Pero aún hay más vías y una de ellas es la que Pedro García investiga en su laboratorio del CSIC: el uso de virus capaces de devorar bacterias o bacteriófagos. El científico explica que esta es una de las más promisorias vías con las que se cuenta para hacer frente a las superbacterias, "pues permite diseñar tratamientos específicos". El mecanismo es sencillo: "El virus se introduce, infecta la bacteria y codifica una enzima que acaba rompiendo su pared, lo que permite al virus salir en busca de más células bacterianas que neutralizar". Esa enzima con propiedades antibióticas, también conocidad como enzibiótico, puede ser la próxima gran arma de la medicina contra las superbacterias.