¿Qué se sabe de Hipra, la vacuna made in Spain?
El lunes buscarán a los primeros voluntarios.
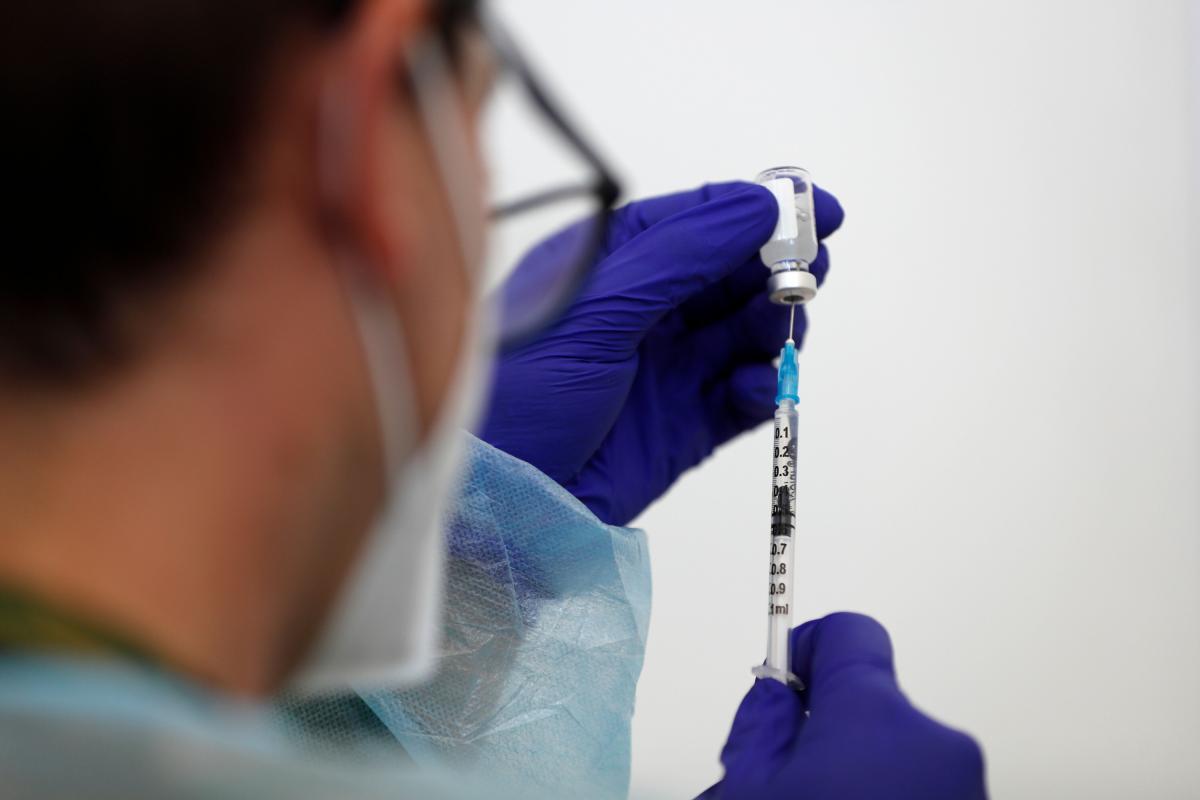
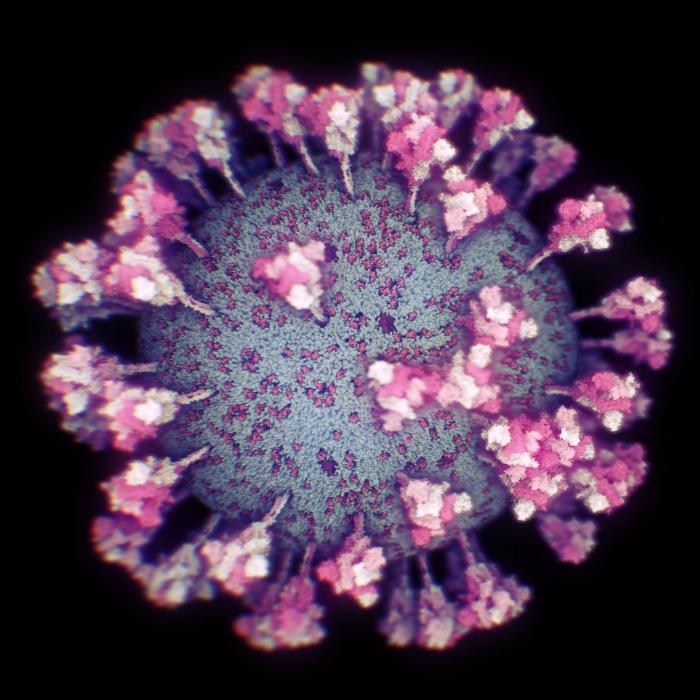
España entra en la carrera contra la Covid-19 con su primera vacuna de producción nacional. La Agencia Estatal de Medicamentos y Productos Sanitarios (AEMPS) ha autorizado este lunes el ensayo clínico de las dosis de PHH-1V del laboratorio Hipra. ¿Qué se sabe hasta el momento de la primera vacuna española?
¿Qué es HIPRA?
Es una farmacéutica española dedicada a salud animal líder en vacunas veterinarias. Sin embargo la compañía creó una división de salud humana para contribuir a paliar la pandemia. Su oficina central está en la localidad de Amer (Girona) y cuenta con filiales y distribuidores en todos los continentes.
Desde el primer momento, la empresa ha contado con el apoyo de ayudas públicas, con ayudas de la Comisión Europea, con asesoría por parte de la AEMPS y sinergias con hospitales e institutos de investigación.
La vacuna
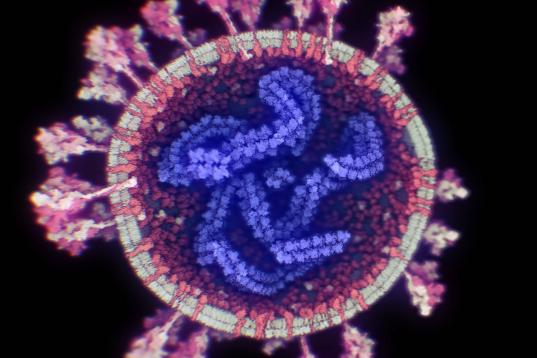
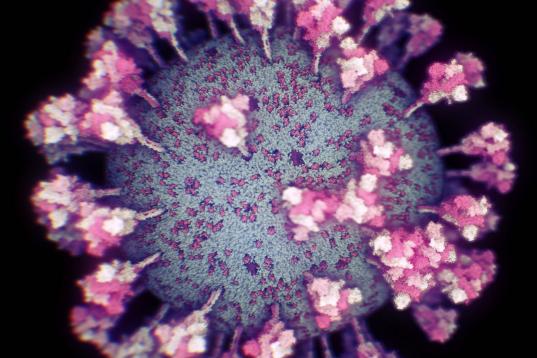
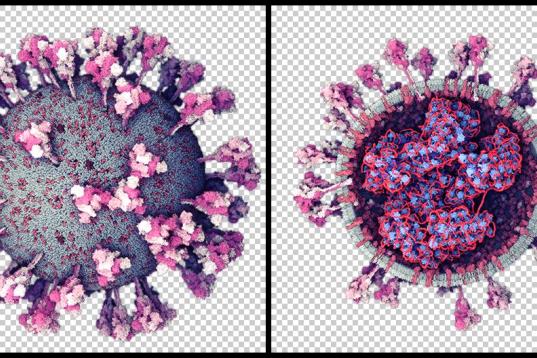
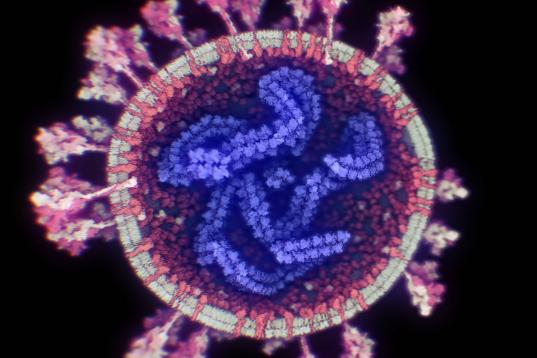
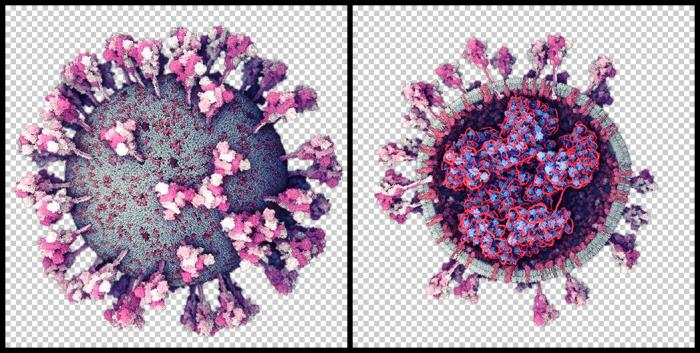
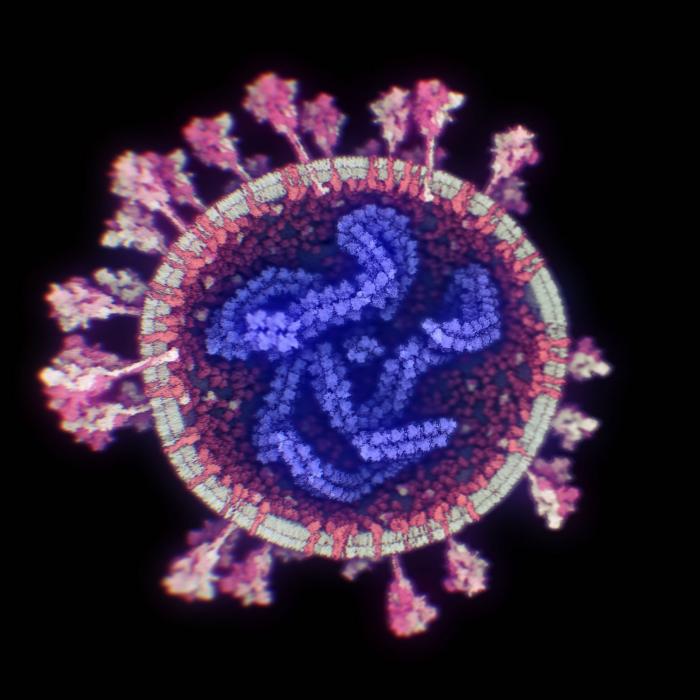
La diferencia con otras es que está basada en dos proteínas del virus que se unen, en vez de otras que usan su material genético. Una proteína corresponde a la variante alfa y la otra a la variante beta y juntas forman una estructura única llamada dímero y que se acompañan de un adyuvante que incrementa la respuesta inmunológica. Esta combinación es capaz de generar una respuesta inmunológica frente a una de las proteínas del virus SARS-CoV-2, conocida como proteína S (spike o de espiga, en español).
¿Es resistente a las nuevas variantes?
La ministra de ciencia, Diana Morant, ha confirmado en La Ventana de Cadena SER que la vacuna ha sido diseñada teniendo en cuenta su protección frente a las nuevas variantes.
Respecto a la combinación con otras vacunas existentes, Morant ha explicado que solo se podrá confirmar cuando concluya la evidencia científica.
Por su parte, el director de la división de Salud Humana de la farmacéutica, Toni Maneu, ha explicado a la agencia Efe que se ha trabajado con la estrategia de que esta vacuna sirca como dosis de recuerdo.

El primer ensayo con humanos
Se trata de un ensayo fase I/IIa de escalada de dosis, que administra la vacuna u otra autorizada enmascarada (ni el paciente ni el equipo sabe cuál se inyecta) en dos fases de forma aleatoria y controlada.
El proceso comienza con la división de los voluntarios en grupos (cohortes) y se empezará administrando la dosis más baja a la primera cohorte. Tras su evaluación por parte de un comité independiente de vigilancia de los datos de seguridad, se irán escalando las dosis siguientes si no se han detectado problemas.
En esta fase se va determinar su inmunología, eficacia, la dosis adecuada y los efectos secundarios.
¿Quién puede participar?
Se reclutará a varias decenas de voluntarios de los hospitales Trueta de Girona y del Clínic de Barcelona de entre 18 y 39 años. Cada participante recibirá dos inmunizaciones separadas por 21 días.
En una segunda fase, que iniciará dentro de un mes y medio se involucrarán otros centros hospitalarios de España y también de Italia y Portugal.
¿Cuándo se iniciará?
Una vez que la AEMPS ha dado luz verde al ensayo clínico, el laboratorio ha señalado que este lunes iniciarán el proceso de selección de los voluntarios para que el ensayo empiece cuanto antes.
Gran capacidad de producción
Si los ensayos concluyen con éxito, HIPRA podrá comenzar la producción en octubre con el objetivo de que se comercialice a finales de 2021, sujeto a la obtención de las autorizaciones correspondientes.
Se espera que Hipra produzca 400 millones de dosis durante el próximo año y que podría ampliarse a 1.200 millones de dosis en 2023.
Sin congelación
Una de las ventajas que tiene la vacuna española es que las dosis se conservarán entre 2ºC y 8ºC, por lo que no requiere congelación y esto facilitará su logística y distribución.
Otras opciones españolas en cola
Hipra también está llevando a cabo una investigación en colaboración con el hospital Clínic de Barcelona para el desarrollo de una vacuna basada en el ARN del virus.
A este proyecto se suma el que está trabajando el equipo de Mariano Esteban y Juan García Arriaza en el CSIC y que está a la espera de recibir la aprobación de la AEMPS para comenzar los ensayos en voluntarios después de mostrar una eficacia del 100% en ratones. La compañía biotecnológica española Biofabri, del grupo Zendal, esta fabricando el prototipo y colaborando con el CSIC.
Otros proyectos en proceso son el de Luis Enjuanes e Isabel Sola que desarrollan una vacuna con la copia sintética casi completa del virus. Y el de Vicente Larraga que consiste en colocar un gen de un antígeno del virus en un vehículo sintético de ADN que pueda introducirse en el paciente y protegerlo frente a la infección.